深海碳是如何被铁固定的?可以稳定长期储存吗?
海洋是地球上最大的碳库之一,通过生物碳泵等方式输送到深海,在海底沉积物中,碳竟然可以被铁矿物吸附锁住,结合形成的铁结合有机碳更难被微生物分解,研究估算,全球海洋表层沉积物中,约20%的有机碳是以Fe-OC的形式存在的,它们是怎么固定的?可以稳定长期储存吗?
海洋沉积物中的铁结合有机碳
海洋沉积物是有机碳长期埋藏的最大净汇,每年约有2亿吨碳以这种方式被埋葬,然而,平均有87%到达海底的有机碳会在沉积物-水界面被再矿化,被微生物分解,仅有少部分能够长期封存。
而有研究发现,活性铁竟然可以增加海底碳封存比例,通过物理保护和抑制微生物降解,铁与碳的结合形成OC-Fe,可以显著提升碳的埋藏效率,在第第四纪陆地沉积物中约40%的有机碳以OC-Fe的形式保存。
活性铁主要以铁(氢)氧化物形式存在,如铁铁矿、针铁矿,其保护有机碳的机制可分为吸附作用、共沉淀作用和多层覆盖三类。吸附作用是指有机分子通过羧基等功能团与铁矿物表面形成内层配位键Fe-O-C;共沉淀作用是指有机碳与铁在氧化还原边界,如海洋沉积物中的有氧-无氧过渡带同时沉淀,形成更稳定的复合体,深海洋沉积物中以此机制为主;而多层覆盖则是指有机质通过疏水作用或阳离子桥接包裹铁矿物,形成物理屏障,主要在陆域土壤中。
通过蒙特卡洛模型估算,全球海洋每年通过OC-Fe埋藏的碳量为31~70Mt C/yr,平均为52Mt C/yr,占海洋总碳埋藏的25%。主要场所包括大陆架与斜坡、三角洲/河口和火山灰沉积区。值得注意的是,缺氧盆地的OC-Fe更高。就OC-Fe固碳而言,陆地埋藏量远超海洋,年均为146-917 Mt C/yr,平均为446Mt C/yr。
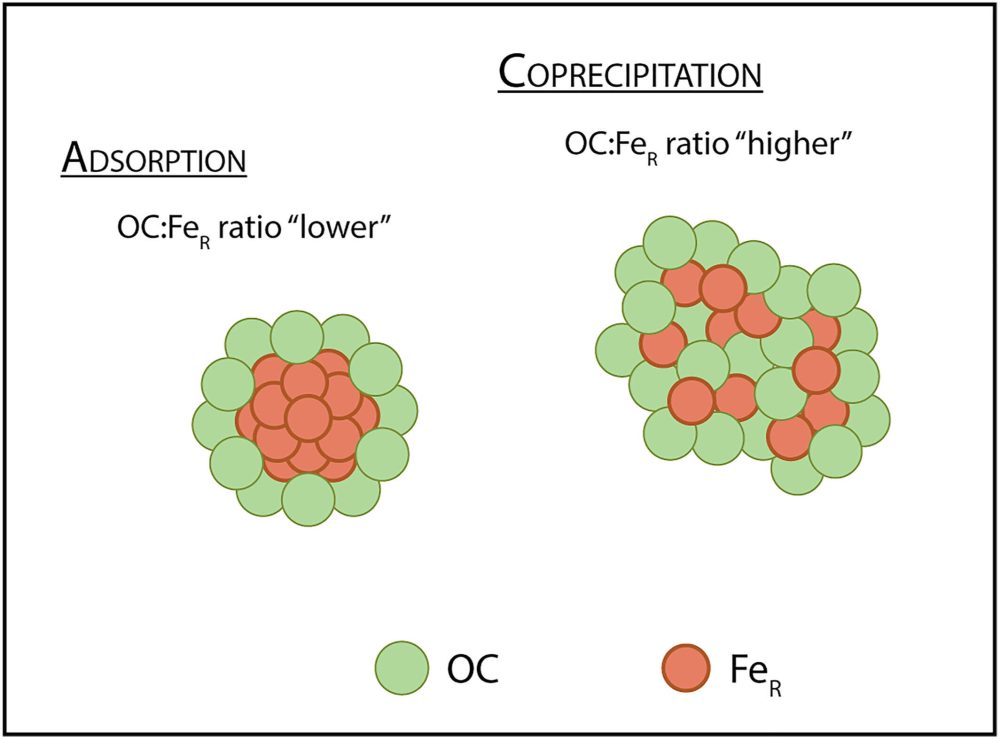
图:两种结合机制示意图🔽
第一种是吸附,即有机碳 (OC) 化合物附着在活性 Fe 表面,这一过程导致 OC:Fe R比降低。第二种是共沉淀,即 OC 和 Fe R同时沉淀,导致 OC:Fe R比升高。
深海铁结合有机碳长期稳定吗?
这种OC-Fe结合物理理论上可以长期保存数十万年,然而这些铁锁碳在深海沉积物中会一直稳定存在吗?深海沉积物是地球上最缺乏能量的环境之一,但微生物依然顽强生存,Fe-OC是否可以作为微生物的能量来源呢?
我们知道,在海底沉积物深处,存在一个特殊的区域,叫硫酸盐-甲烷过渡带,这里,甲烷氧化菌和硫酸盐还原菌合作,利用甲烷作为能源,同时消耗硫酸盐。而在这个过程中,铁矿物可能被分解。
某些硫酸盐还原菌能把三价铁Fe³⁺还原成二价铁Fe²⁺,释放出原本锁住的碳;此外,微生物产生的硫化氢也可能会溶解铁矿物,让铁固定的碳溢出。
研究团队在南海北部钻取了两个沉积物岩芯,QDN-G1和QDN-14B,研究发现,在硫酸盐-甲烷过渡带,Fe-OC含量显著下降。在正常沉积物中,Fe-OC占总有机碳的的13%左右,而在QDN-14B中仅5.2%,表明部分碳被释放了。
计算表明:在硫酸盐-甲烷过渡带甲烷活跃的QDN-14B岩芯中,Fe-OC贡献了36.7%的碳再矿化量,而在普通深海沉积物QDN-G1岩芯中,这一比例只有10%–23%。
虽然硫酸盐-甲烷过渡带中部分Fe-OC被释放,但从整体来看,铁依然是碳的重要固碳源。在非硫酸盐-甲烷过渡带沉积物中,Fe-OC占比稳定在13.3%左右,即使沉积物年龄超过10万年,这一比例仍变化不大。而且,在深海主要以共沉淀形式结合,这种更难被降解。
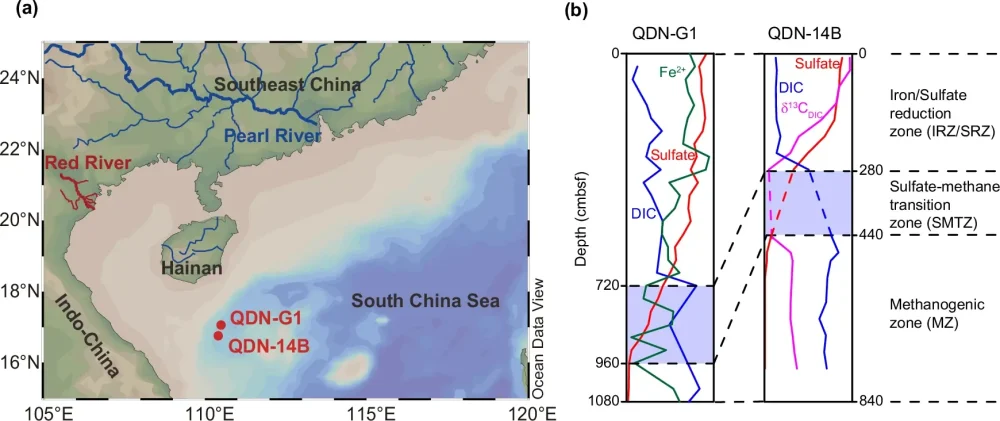
图:南海北部研究岩心图及其生物地球化学分带🔽
a QDN-G1 和 QDN-14B 岩芯图。流入南海北部的河流系统用蓝线和红线表示。b根据孔隙水地球化学推断的 QDN-G1 和 QDN-14B 岩芯生物地球化学分带示意图,包括铁还原带 (IRZ)、硫酸盐还原带 (SRZ)、硫酸盐-甲烷过渡带 (SMTZ) 和产甲烷带 (MZ)。Fe(II) 浓度、硫酸盐浓度、溶解无机碳 (DIC) 浓度和 DIC 碳同位素比 (δ 13 C DIC ) 分别以绿线、红线、蓝线和洋红色线表示。SMTZ 的位置以紫色突出显示。QDN-14B 的孔隙水地球化学数据来自 Niu et al., 2017 和 Hu et al., 2019 28,60 。详细的孔隙水地球化学数据绘制在补充图 2和3中。源数据以源数据文件的形式提供。
❓思考题:在海洋沉积物中,铁矿物可以固定多少比例的有机碳?
A.5%
B.10%
C.20%
D.50%
参考答案:(点击查看)
C.
解析:研究发现,全球海洋表层沉积物中约20%的有机碳是以铁结合有机碳的形式存在的。
参考文献:Yunru Chen, Liang Dong, Weikang Sui, Mingyang Niu, Xingqian Cui, Kai-Uwe Hinrichs, Fengping Wang. Cycling and persistence of iron-bound organic carbon in subseafloor sediments. Nature Communications, 2024; 15 (1) DOI: 10.1038/s41467-024-50578-5
